- Muallif Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:52.
- Oxirgi o'zgartirilgan 2025-06-01 07:38.
Uglerod kislotasi va bikarbonat oʻrtasidagi asosiy farq shundaki, karbonat kislota neytral kimyoviy birikma, bikarbonat esa manfiy zaryadlangan kimyoviy birikma.
Karbonat kislotasi H2CO3 kimyoviy formulasi bilan karbonat angidrid suvda eriganida eritmada hosil boʻladigan kuchsiz kislota. Bikarbonat uchta kislorod atomi, vodorod atomi va HCO3- kimyoviy formulali uglerod atomining birikmasidan hosil bo'ladi.
Karbon kislotasi nima?
Karbon kislotasi H2CO3. Ba'zan biz bu nomni suvda yoki gazlangan suvda erigan karbonat angidridga ega bo'lgan eritmalarga beramiz. Buning sababi shundaki, gazlangan suvda oz miqdorda H2CO3 mavjud. Bundan tashqari, karbonat kislota zaif kislotadir va u karbonatlar va bikarbonatlar kabi ikki turdagi tuzlarni hosil qilishi mumkin. Ushbu birikmaning molyar massasi 62,024 g/mol.
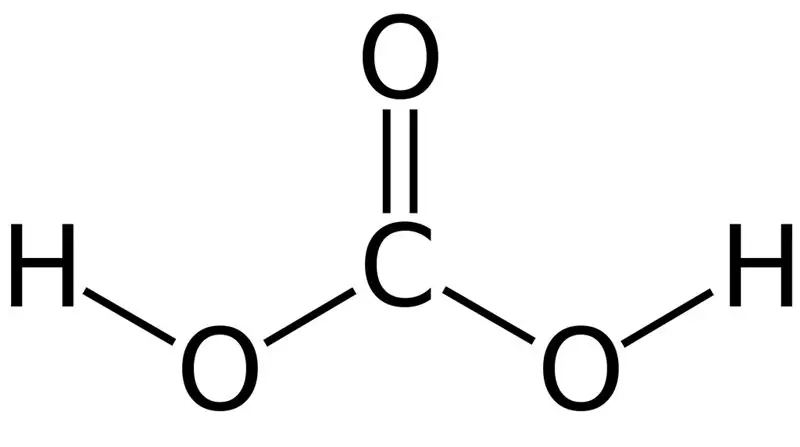
01-rasm: Karbon kislotaning kimyoviy tuzilishi
Karbonat angidrid suvda eriganda, karbonat angidrid va karbonat kislotasi oʻrtasidagi muvozanatga kiradi. Muvozanat quyidagicha:
CO2 + H2O ⟷ H2CO3
Agar asosga ortiqcha karbonat kislota qo'shsak, u bikarbonat beradi. Ammo, agar asos ortiqcha bo'lsa, u holda karbonat kislotasi gazlangan tuzlarni berishga intiladi. Aniqroq aytganda, karbonat kislotasi karbonil uglerodga biriktirilgan ikkita gidroksil guruhi o'rnini bosuvchi karboksilik kislota birikmasidir. Bundan tashqari, bu protonlarni berishga qodir bo'lgan poliprotik kislota. U ikkita olinadigan protonga ega, shuning uchun u diprotikdir.
Bikarbonat nima?
Bikarbonat uchta kislorod atomi, vodorod atomi va uglerod atomining birikmasidan hosil bo'ladi. Ushbu birikmaning mahsuloti ion yoki protonlardan ko'ra ko'proq elektronli birikma bo'lishi mumkin. Biz uni HCO3- kimyoviy formulasiga ega kimyoviy tur sifatida tasvirlashimiz mumkin.
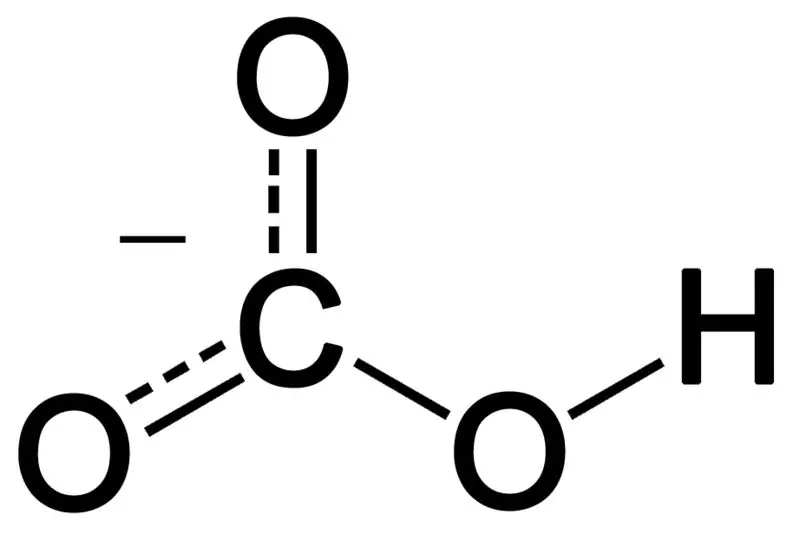
02-rasm: Bikarbonat anionining kimyoviy tuzilishi
Bu birikma oddiy tilda aytganda, tananing pH tamponlash tizimining muhim qismidir: u qonni juda kislotali yoki juda asosli bo'lmagan holatda saqlash uchun javobgardir. Bundan tashqari, u oshqozon ovqatni hazm qilishni tugatgandan so'ng, ovqat hazm qilish sharbatini nazorat qilish usuli sifatida xizmat qiladi. Bundan tashqari, yomg'ir suvidagi karbonat kislotasi toshlarga urilganda bikarbonat ionlarini hosil qiladi. Bikarbonat ionlarining bu oqimi uglerod aylanishini davom ettirishda muhim ahamiyatga ega.
Karbonat kislota va bikarbonat oʻrtasidagi farq nima?
Karbonat kislotasi kuchsiz kislota boʻlib, karbonat angidrid suvda eriganda eritmada hosil boʻladi va kimyoviy formulasi H2CO3. Bikarbonat uchta kislorod atomi, vodorod atomi va HCO3- kimyoviy formulali uglerod atomining birikmasidan hosil bo'ladi. Karbonat kislotasi va bikarbonat o'rtasidagi asosiy farq shundaki, karbonat kislota neytral kimyoviy birikma, bikarbonat esa manfiy zaryadlangan kimyoviy birikma. Bundan tashqari, karbonat kislotasi ko'pikli, gazlangan ichimliklar tayyorlashda, dermatitlarni davolashda, og'izni yuvishda va hokazolarda, bikarbonat esa pishirish kabi oziq-ovqat preparatlarida (achituvchi vosita sifatida) ishlatiladi va pH o'zgarishiga qarshilik ko'rsatish qobiliyatini beradi.
Quyidagi infografikada uglerod kislotasi va bikarbonat oʻrtasidagi farq jadval koʻrinishida keltirilgan.
Xulosa - karbonat kislota va bikarbonat
Karbon kislotasi H2CO3. Bikarbonat HCO3- kimyoviy formulasi bilan uchta kislorod atomi, vodorod atomi va uglerod atomining birikmasidan hosil bo'ladi. Karbonat kislota va bikarbonat o'rtasidagi asosiy farq shundaki, karbonat kislota neytral kimyoviy birikma, bikarbonat esa manfiy zaryadlangan kimyoviy birikma.






